
DIAGNÓSTICO Y REFUERZO

- La actividad Diagnóstica consta de 4 partes: taller de repaso en clase, Revisión de temas a nivel virtual en las páginas sugeridas, socialización en clase y EVALUACIÓN virtual.
- Revisión del tema de distribución electrónica. Debes hacer clic donde dice " Actividad No 1". y revisar todos lo link que se sugieren.
- Revisión del concepto de enlace químico y los tipos de enlace, debes hacer clic donde dice " Actividad No 2". Revisar todos los enlaces
- Actividad No 3, en esta parte se busca que practiques estos temas desarrollando algunos ejercicios seleccionados. Se sugiere visitar todos los links que corresponden a recursos educativos abiertos y algunos juegos sugeridos.
EVALUACIÓN DIAGNÓSTICA

- Ingresa haciendo clic aquí y contesta todas las preguntas.
- al final cuando termines das clic en enviar y te saldrá un letrero que dice: Se ha registrado tu respuesta. Gracias.
- Al correo electrónico registrado, se enviara luego de la revisión, la puntuación obtenida, Debes dar clic en ver puntuación y te saldrán las preguntas cuyas respuestas fueron incorrectas
- Copia en el cuaderno las preguntas incorrectas y corrige cada una de ellas con los respectivos procedimientos y explicaciones.
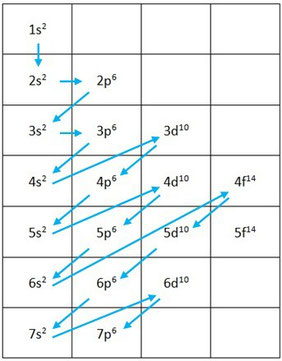
Distribución electrónica
La distribución electrónica consiste en distribuir los electrones en torno al núcleo en diferentes estados energéticos (niveles, subniveles y orbitales).
Primero se realiza la distribución por subniveles, lo que involucra la distribución por niveles; finalmente analizaremos la distribución electrónica por orbitales, la cual se rige por principios.
Tomado de: http://www.fullquimica.com/2012/08/distribucion-electronica.html
!Para Saber más.....!

La manera en que los átomos se enlazan ejerce un efecto profundo sobre las propiedades físicas y químicas de las sustancias. Por ejemplo, al respirar monóxido de carbono, las moléculas de CO se enlazan fuertemente a ciertas sustancias presentes en los glóbulos rojos de la sangre haciendo que estos queden como mineralizados, incapaces de transportar oxígeno, perdiendo así sus propiedades vitales. Entonces debemos preguntarnos: ¿Qué es el enlace químico?, ¿Cómo se da?, ¿Qué lo facilita?, ¿Qué lo impide?, ¿Qué determina que unos sean más fuertes que otros? Estas interrogantes son fundamentales en el estudio de la química, pues los cambios químicos, son esencialmente una alteración de los enlaces químicos.
La materia sufre cambios o-fenómenos - físicos y químicos. Los cambios químicos, en los cuales se modifica la naturaleza de las sustancias que intervienen, reciben el nombre de reacciones químicas.
Tomado de : http://www.oei.org.co/fpciencia/art08.htm
Tomado de: http://www.lamanzanadenewton.com/materiales/aplicaciones/lrq/lrq_rq.html




Samuel Santiago Díaz rojas (jueves, 29 febrero 2024 21:09)
Curso 801
Samuel Santiago Díaz rojas (jueves, 29 febrero 2024 21:09)
Curso 801
Samuel Santiago Díaz rojas (jueves, 29 febrero 2024 21:08)
Curso 801
Samuel Santiago Díaz rojas (jueves, 29 febrero 2024 21:07)
Curso 801